基础化学原料制造 二氧化碳的制取与性质实验设计与实践
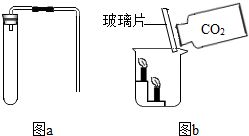
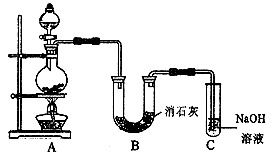
在化学学习与实践中,基础化学原料的制取与性质探究是培养科学素养的重要环节。化学兴趣小组以二氧化碳(CO₂)为例,设计并进行了系统的制取与性质实验,不仅巩固了理论知识,更锻炼了实践操作能力。实验的第一步,如图A所示,是确保实验安全与成功的基础——检查装置的气密性。
一、气密性检查:实验成功的基石
小组同学严格按照规范操作:先将连接好的导管末端浸入盛有水(通常是清水)的烧杯中,然后用手(或使用热毛巾)紧紧握住试管(或锥形瓶等反应容器)的外壁。观察到的关键现象是:导管口有连续、均匀的气泡冒出。当手松开后,一段时间内,导管内会形成一段稳定的水柱。
原理解析: 手握试管,使试管内的空气受热膨胀,内部气压增大。如果装置连接严密、气密性良好,增大的气压就会将空气从导管口压出,形成气泡。松开手后,装置冷却,内部气压减小,外界大气压将水压入导管,形成水柱。这一系列现象证明了装置不漏气,可以安全地进行后续气体生成反应。这一步至关重要,能有效防止反应生成的气体逸散,确保实验的准确性与安全性,是任何涉及气体制造与收集实验的必备前提。
二、二氧化碳的实验室制取:原理与操作
在确认气密性良好后,兴趣小组通常采用经典且安全的实验室制法:
- 药品: 大理石或石灰石(主要成分为碳酸钙,CaCO₃)与稀盐酸(HCl)。
- 原理: 复分解反应:CaCO₃ + 2HCl → CaCl₂ + H₂O + CO₂↑。该反应速率适中,易于控制,生成的二氧化碳较为纯净。
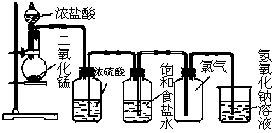
- 装置: 采用“固液常温型”发生装置(即使用带导管的锥形瓶或试管,配长颈漏斗或分液漏斗),采用向上排空气法收集(因CO₂密度大于空气)。
三、二氧化碳性质的探究:验证与应用
制得二氧化碳后,小组设计了一系列实验探究其化学与物理性质:
- 物理性质验证: 将收集满的CO₂气体瓶正放在桌上,放入燃着的木条,木条熄灭,初步证明其不支持燃烧;向一个平衡的天平一端的纸杯(或烧杯)中倾倒CO₂,天平倾斜,直观证明其密度大于空气。
- 化学性质探究:
- 与水反应: 向紫色石蕊试液中通入CO₂,溶液变红,证明CO₂与水反应生成碳酸(H₂CO₃)。加热变红的溶液,红色褪去恢复紫色,证明碳酸不稳定,易分解。
- 与碱反应(核心性质): 向澄清石灰水(氢氧化钙溶液)中通入CO₂,溶液变浑浊,生成白色沉淀(碳酸钙,CaCO₃),这是检验CO₂的特征反应:CO₂ + Ca(OH)₂ → CaCO₃↓ + H₂O。继续通入过量CO₂,沉淀溶解,溶液又变澄清,生成可溶性的碳酸氢钙:CaCO₃ + CO₂ + H₂O → Ca(HCO₃)₂。
四、联系实际:基础化学原料制造的意义
二氧化碳不仅是实验室研究的重要对象,更是一种重要的基础化工原料和产品。在工业上,其制造方法多样,如高温煅烧石灰石(CaCO₃ → CaO + CO₂↑)、合成氨工业的副产气、烟道气回收等。工业级CO₂经纯化、压缩、液化后,广泛应用于:
- 食品行业: 碳酸饮料的添加剂、食品保鲜与冷藏(干冰)。
- 工业生产: 焊接保护气、铸造硬化剂、纯碱(Na₂CO₃)、小苏打(NaHCO₃)、尿素等化工产品的合成原料。
- 农业与科研: 气体肥料、超临界萃取溶剂、灭火剂等。
###
从兴趣小组精心的气密性检查开始,到完整经历CO₂的制取、收集与性质验证,这一过程完美体现了从理论到实践、从基础操作到性质认知的科学探究路径。它不仅是化学学习的生动课堂,更是一次对“基础化学原料制造”的微观模拟与深刻理解。通过这样的实践,同学们不仅掌握了知识与技能,更能体会到化学作为一门中心学科,在连接基础研究与实际工业生产、创造社会价值中的关键作用。严谨的气密性检查,正是这一切探索安全、高效进行的起点与保障。
如若转载,请注明出处:http://www.kongfenjianxiu.com/product/8.html
更新时间:2026-04-29 20:02:44