氯气制备与性质探究实验分析
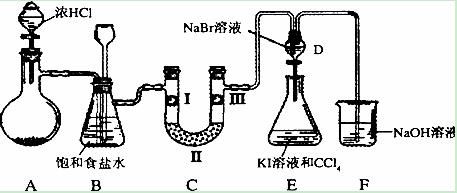
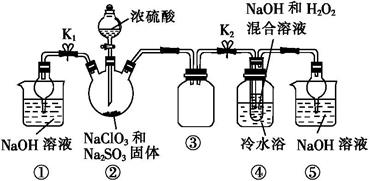
某化学小组设计了以氯酸钾与浓盐酸反应制备氯气,并探究其相关性质的实验装置。以下就题目中提出的两个问题进行具体分析:
1. 关于电子转移物质的量的计算
当装置A中的固体药品为氯酸钾(KClO₃)时,其与浓盐酸反应的化学方程式为:
KClO₃ + 6HCl(浓) = KCl + 3Cl₂↑ + 3H₂O
分析该氧化还原反应:
- 氯酸钾(KClO₃)中氯元素的化合价为+5价,被还原为氯气(Cl₂)中的0价。
* 盐酸(HCl)中氯元素的化合价为-1价,部分被氧化为氯气(Cl₂)中的0价。
从方程式看,生成3 mol Cl₂时,有1 mol Cl来自KClO₃(得5 mol电子被还原),有5 mol Cl来自HCl(失5 mol电子被氧化)。因此,整个反应中电子转移的总物质的量为 5 mol。
所以,反应中每生成3 mol Cl₂时,转移电子的物质的量为 5 mol。
2. 关于装置B的作用与工业应用
装置B在此实验流程中主要起除杂作用。由于制备氯气所用的浓盐酸易挥发,产生的氯气中会混有氯化氢(HCl)气体和水蒸气。
- 除去氯化氢:通常装置B中盛有饱和食盐水(NaCl溶液)。根据同离子效应,高浓度的氯离子(Cl⁻)可以显著降低HCl在溶液中的溶解度,从而使氯气通过时,氯化氢被吸收溶解,而氯气损失较少。
- 基础化学原料制造中的意义:氯气是重要的基础化工原料。通过此类实验装置获得的相对纯净的氯气,在工业生产中可用于制造一系列下游产品,例如:
- 合成氯化氢(HCl)及盐酸。
- 生产次氯酸钠(NaClO)、漂白粉等含氯消毒剂和漂白剂。
- 用于有机合成,生产氯代烃、聚氯乙烯(PVC)等。
* 用于金属冶炼和提纯。
因此,装置B的除杂步骤是确保后续反应或产品纯度的重要环节,是实验室制备与工业化生产中连接基础原料与高端制造的关键预处理操作。
该实验设计有效地结合了氯气的制备、净化与性质探究,体现了从理论到应用的化学研究思路。
如若转载,请注明出处:http://www.kongfenjianxiu.com/product/19.html
更新时间:2026-04-29 06:32:35