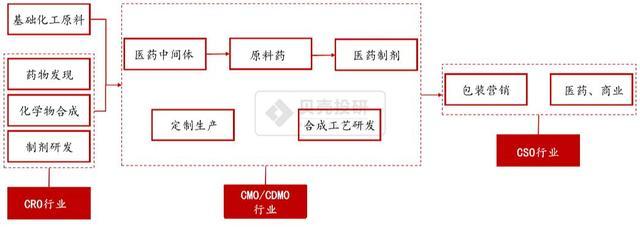
氯化亚锡 (Stannous Chloride) 综合概述 从基础物化性质到工业应用
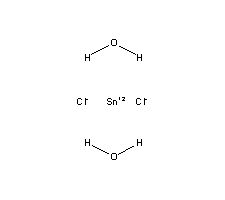
氯化亚锡,又称二氯化锡,是一种重要的无机化合物,在基础化学原料制造领域扮演着关键角色。以下是对其各项特性的综合阐述。
一、 基本信息
中文名: 氯化亚锡 / 二氯化锡
英文名: Stannous Chloride / Tin(II) Chloride
分子式: SnCl₂
分子量: 189.60 g/mol (无水物)
结构式: 为离子化合物,晶体结构中Sn²⁺离子被Cl⁻离子包围。无水物为链状聚合物结构,二水合物(SnCl₂·2H₂O)为分子晶体。
CAS号: 无水物:7772-99-8;二水合物:10025-69-1
二、 物理性质
外观: 无水物为白色或无色结晶性固体;常见的二水合物(SnCl₂·2H₂O)为无色针状或片状结晶。
熔点: 无水物约247°C;二水合物约37.7°C (在其结晶水中熔化)。
沸点: 无水物约623°C分解。
溶解性: 易溶于水,并发生强烈水解产生白色沉淀(碱式氯化亚锡)。易溶于乙醇、丙酮、乙醚等有机溶剂。其水溶液因水解而呈酸性。
三、 化学性质
1. 还原性: 氯化亚锡最突出的化学性质是强还原性,能将许多金属离子(如Fe³⁺、Hg²⁺、Cu²⁺)还原至低价态,自身被氧化为Sn⁴⁺。是分析化学和有机合成中常用的温和还原剂。
2. 水解性: 在水中发生强烈水解:SnCl₂ + H₂O → Sn(OH)Cl↓ + HCl。因此,配制其溶液时需先用浓盐酸溶解以抑制水解。
3. 配位性: Sn²⁺是良好的路易斯酸,能与Cl⁻、OH⁻等配体形成配合物,如[SnCl₃]⁻、[Sn(OH)₃]⁻等。
4. 不稳定性: 在空气中易被氧化,水溶液更易被氧化,需密封保存并常加入锡粒防止氧化。
四、 制备方法
工业上主要采用以下方法:
1. 锡与盐酸反应: 将金属锡溶于热的浓盐酸中,反应生成SnCl₂·2H₂O,经蒸发、冷却结晶可得二水合物。
> Sn + 2HCl → SnCl₂ + H₂↑
2. 锡与氯气反应: 在严格控制条件下,使熔融锡与干燥氯气反应,可制得无水氯化亚锡。
> Sn + Cl₂ → SnCl₂
- 氯化亚锡溶液的浓缩结晶: 从含锡废料中回收,通过酸溶、还原、净化、浓缩等步骤制备。
五、 主要用途
氯化亚锡作为基础化学原料,用途广泛:
- 还原剂: 用于化学分析(如汞、钼的测定)、有机合成(如硝基还原为氨基)、染料合成。
- 电镀工业: 作为酸性镀锡和合金电镀(如锡-锌、锡-钴)的主盐和添加剂。
- 媒染剂: 在纺织品染色和印花中作为媒染剂。
- 稳定剂: 用于聚氯乙烯(PVC)塑料的稳定剂(与铅、镉盐协同)。
- 其他: 制造其他锡盐的原料、玻璃表面处理、润滑油添加剂等。
六、 安全性与毒性
毒性: 属中等毒性。对眼睛、皮肤和呼吸道有刺激性。摄入有毒。长期或反复接触可能对器官造成损害。
MSDS (物质安全数据表) 要点: 其MSDS通常标明其为腐蚀性、刺激性物质,要求操作时佩戴防护装备(手套、护目镜、防尘口罩),确保良好通风。储存于阴凉、干燥、通风处,远离氧化剂。泄漏时需用惰性材料吸收,按危险废物处置。
七、 供应商与公司
氯化亚锡作为常用化工原料,在全球范围内有许多生产商和供应商。知名公司包括(此处为示例,不构成采购建议):
- 国际: 西格玛奥德里奇(Sigma-Aldrich,现默克生命科学)、赛默飞世尔(Thermo Fisher Scientific)、巴斯夫(BASF)等。
- 中国: 国内众多精细化工企业均有生产,如云南锡业、广西华锡、以及江苏、湖南、广东等地的大型化工原料生产贸易公司。采购时可通过专业的化学品B2B平台或直接联系生产商获取具体信息。
氯化亚锡以其独特的还原性和其他化学性质,成为连接金属锡与下游众多应用领域的关键基础原料之一,在化工、电镀、分析、纺织等行业中不可或缺。
如若转载,请注明出处:http://www.kongfenjianxiu.com/product/16.html
更新时间:2026-04-29 08:06:24