实验室制备纯净干燥氯气的原理与装置设计
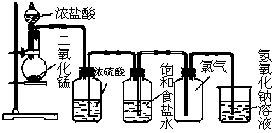
在化学实验室中,利用二氧化锰与浓盐酸反应是制备氯气的一种经典方法。该方法操作相对简便,原料易得,是学习和验证氯气性质的基础实验。
1. 反应的化学方程式
该反应属于氧化还原反应,二氧化锰作为氧化剂,浓盐酸作为还原剂和反应介质。反应的化学方程式为:
MnO₂ + 4HCl(浓) → MnCl₂ + Cl₂↑ + 2H₂O
值得注意的是,此反应需要加热条件才能顺利进行,且必须使用浓盐酸。若盐酸浓度过低,反应将难以发生或进行不完全。
2. 实验装置设计与净化流程分析
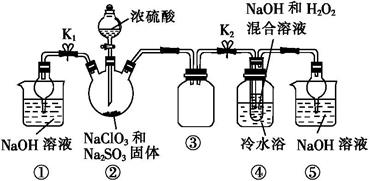
一个设计合理的实验装置是成功制备纯净、干燥氯气的关键。一套完整的装置通常包括以下几个部分:
(1)气体发生装置
通常采用“固+液加热型”气体发生装置,即在圆底烧瓶或锥形瓶中放入二氧化锰固体,通过分液漏斗滴加浓盐酸,并用水浴或酒精灯加热(注意避免局部过热)。
(2)气体净化装置
从发生装置中导出的氯气含有杂质,主要是挥发出来的氯化氢气体和水蒸气。因此,气体需要依次通过两个洗气瓶进行净化:
- 除氯化氢(HCl):将气体通入盛有饱和食盐水的洗气瓶。由于氯气在饱和食盐水中的溶解度远小于氯化氢,此法可有效除去大部分氯化氢。
- 除水蒸气(干燥):将气体通入盛有浓硫酸的洗气瓶。浓硫酸是高效的干燥剂,能吸收氯气中残留的水分,得到干燥的氯气。
(3)气体收集装置
干燥纯净的氯气密度大于空气,且能溶于水,因此通常采用向上排空气法收集。导气管应伸入集气瓶底部,利用氯气将瓶内空气向上排出。也可将氯气通入排饱和食盐水法收集,以减少其溶解损失。
(4)尾气处理装置
氯气有毒,不能直接排放到空气中。多余的氯气必须进行吸收处理。通常将尾气通入盛有氢氧化钠溶液的烧杯中,发生反应:Cl₂ + 2NaOH → NaCl + NaClO + H₂O,从而被有效吸收。
与安全提示
整个实验装置的设计应遵循“发生→净化→干燥→收集→尾气处理”的连贯流程,各部件之间导管连接要严密,气流方向正确。实验中需特别注意:
- 加热温度不宜过高,防止盐酸过度挥发。
- 严格遵守实验操作规范,在通风橱内或通风良好的环境下进行。
- 检查装置气密性,防止氯气泄漏。
- 准备好防护用具,如橡胶手套和护目镜。
通过这个系统的实验,不仅能成功制得纯净干燥的氯气,还能深刻理解气体制备、净化、收集及尾气处理的全套思路,是基础化学原料制造原理在实验室中的典型体现。
如若转载,请注明出处:http://www.kongfenjianxiu.com/product/21.html
更新时间:2026-04-29 02:59:46