工业盐核心成分亚硝酸钠的实验室制备探究
亚硝酸钠(NaNO2)作为一种重要的基础化学原料,在工业生产中扮演着多重角色。它不仅是工业盐的主要成分,还因其独特的化学性质,在漂白、电镀、金属热处理以及食品加工(作为限量的防腐剂和发色剂)等领域有着广泛的应用。
在实验室层面,我们可以通过一套相对简易的装置,以木炭(主要成分为碳,C)、浓硝酸(HNO3)和过氧化钠(Na2O2)为主要原料来制备亚硝酸钠。其核心原理是利用碳与浓硝酸反应生成氮氧化物(主要是NO2),再将其与过氧化钠反应,最终得到目标产物。
反应原理与装置流程
1. 氮氧化物的生成:在加热条件下,木炭(碳)与浓硝酸发生氧化还原反应,生成二氧化碳(CO2)、二氧化氮(NO2)和水。此步骤通常在圆底烧瓶中进行,需要酒精灯加热。反应方程式可简化为:
C + 4HNO3(浓) → CO2↑ + 4NO2↑ + 2H2O
- 气体的净化与干燥:生成的混合气体(CO2和NO2)中可能含有挥发出的硝酸酸雾和水蒸气。气体通过盛有浓氢氧化钠(NaOH)溶液的洗气瓶,可以吸收酸雾和部分CO2。随后通过盛有浓硫酸(H2SO4)或无水氯化钙(CaCl2)的干燥管进行干燥,得到较为纯净、干燥的NO2(可能含部分CO2)。
3. 亚硝酸钠的合成:干燥的NO2气体被导入盛有过氧化钠(Na2O2)固体的硬质玻璃管或反应器中。过氧化钠具有强氧化性,能与NO2反应生成亚硝酸钠和氧气。这是制备的关键步骤,反应方程式为:
Na2O2 + 2NO2 → 2NaNO2 + O2
注意:过氧化钠需保持干燥,且此反应可能较为剧烈,需控制气流速度。
- 尾气处理:未完全反应的氮氧化物(NO、NO2等)有毒,不能直接排放。尾气应通入盛有氢氧化钠溶液的吸收瓶中,被吸收处理,防止污染空气。
实验装置与操作要点
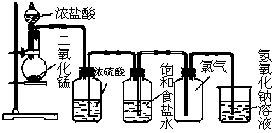
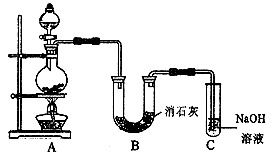
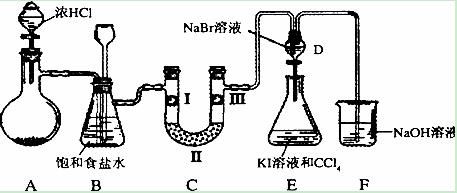
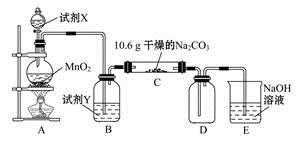
一套完整的制备装置(如图所示,通常从左至右连接)应包括:
- 气体发生装置:圆底烧瓶(装木炭与浓硝酸)、分液漏斗(滴加浓硝酸)、酒精灯。
- 净化干燥装置:洗气瓶(装NaOH溶液)、干燥管(装固体干燥剂)。
- 主反应装置:硬质玻璃管(装Na2O2),可能需要适当加热(但Na2O2与NO2的反应常可常温进行,具体依设计而定)。
- 尾气吸收装置:洗气瓶(装NaOH溶液)。
关键操作与注意事项:
1. 装置气密性必须良好。
2. 浓硝酸具有强腐蚀性,木炭与浓硝酸的反应需在通风橱内或良好通风条件下进行,加热需缓慢。
3. 过氧化钠是强氧化剂,易潮解,应密封保存,取用迅速。与NO2反应时注意安全。
4. 实验结束后,应先撤除加热源,并持续通入惰性气体(如N2)一段时间,确保系统内的有毒气体被完全排出和吸收。
###
通过上述以木炭、浓硝酸和过氧化钠为原料的实验室制备方法,我们不仅能够获得亚硝酸钠样品,更深刻地理解了从基础化学原料制造重要工业产品的化学原理与过程。整个过程涉及气体的生成、净化、反应与尾气处理,是对综合实验能力的良好训练。该实验也警示我们,亚硝酸钠虽用途广泛,但具有一定毒性(尤其在酸性条件下可能生成致癌的亚硝胺),其生产、储存和使用都必须严格遵守安全规范。
如若转载,请注明出处:http://www.kongfenjianxiu.com/product/4.html
更新时间:2026-04-29 19:51:51